制取氧氣的方法:高錳酸鉀制備氧氣,藥品:高錳酸鉀(暗紫色固體)、與二氧化錳(黑色粉末)。高錳酸鉀熱分解的方程式存在爭(zhēng)議,因?yàn)槠湓诓煌瑴囟葪l件下的分解產(chǎn)物會(huì)有差異。二氧化錳與氯酸鉀共熱,氯酸鉀(白色固體)與二氧化錳(黑色粉末)。

1、高錳酸鉀制備氧氣,藥品:高錳酸鉀(暗紫色固體)、與二氧化錳(黑色粉末)。高錳酸鉀熱分解的方程式存在爭(zhēng)議,因?yàn)槠湓诓煌瑴囟葪l件下的分解產(chǎn)物會(huì)有差異。
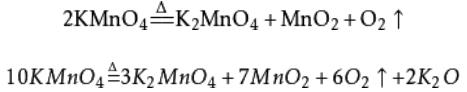
2、二氧化錳與氯酸鉀共熱,氯酸鉀(白色固體)與二氧化錳(黑色粉末)。制得的氧氣中含有少量Cl2、O3和微量ClO2;部分教材已經(jīng)刪掉該制取方法;該反應(yīng)實(shí)際上是放熱反應(yīng),而不是吸熱反應(yīng),發(fā)生上述1mol反應(yīng),放熱108kJ。
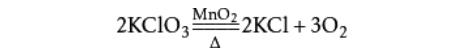
3、過(guò)氧化氫溶液催化分解,藥品:過(guò)氧化氫(H2O2)和二氧化錳(黑色粉末MnO2)。
![]()
氧的相對(duì)原子質(zhì)量是16.00。氧元素符號(hào)O,位于元素周期表第二周期ⅥA族,它也是一個(gè)高反應(yīng)性的第2周期非金屬元素,很容易與幾乎所有其它元素形成化合物(主要為氧化物)。
氧元素符號(hào)O,位于元素周期表第二周期ⅥA族。1774年英國(guó)科學(xué)家約瑟夫·普里斯特利用透鏡把太陽(yáng)光聚焦在氧化汞上,發(fā)現(xiàn)一種能強(qiáng)烈?guī)椭紵臍怏w。
氧氣是一種化學(xué)性質(zhì)比較活潑的氣體,它可以與金屬、非金屬、化合物等多種特物質(zhì)發(fā)生氧化反應(yīng)表現(xiàn)為緩慢氧化、燒、爆等。空氣中可燃燒的物質(zhì),在氧氣中燃燒得更劇烈,而某些在空氣中不燃燒的物質(zhì),在氧氣中也可以發(fā)生燃燒。

氯酸鉀制取氧氣的化學(xué)方程式:2KClO3=(MnO2△)=2KCl+3O2↑。氯酸鉀是強(qiáng)氧化劑。如有催化劑等存在,在較低溫度下就能分解而強(qiáng)烈...

鐵在氧氣中燃燒的化學(xué)方程式為3Fe+2O?=Fe?O?(點(diǎn)燃)。鐵在氧氣中燃燒,反應(yīng)物為鐵和氧氣、生成物為黑色固體四氧化三鐵。在高溫時(shí),鐵在...

鎂和稀鹽酸反應(yīng)的化學(xué)方程式:Mg+2HCl(稀)=MgCl2+H2↑。鎂和稀鹽酸反應(yīng)生成氯化鎂和氫氣氣體,反應(yīng)現(xiàn)象為鎂固體溶解,溶液內(nèi)產(chǎn)生氣...

氫氣還原氧化鐵的化學(xué)反應(yīng)方程式為:Fe?O?+3H?==高溫==2Fe+3H?O,現(xiàn)象是紅褐色固體粉末變成黑色。利用具有半導(dǎo)體特性的氧化鐵等...

濕法煉銅的化學(xué)方程式:1.CuO+H2SO4=CuSO4+H2O基本反應(yīng)類型:復(fù)分解反應(yīng);2.CuSO4+Fe=Cu+FeSO4基本反應(yīng)類型...

稀鹽酸除鐵銹的化學(xué)方程式為:Fe?O?+6HCl═2FeCl?+3H?O,反應(yīng)現(xiàn)象:鐵銹消失,溶液由無(wú)色變?yōu)辄S色。稀鹽酸是質(zhì)量分?jǐn)?shù)低于20%...

氫氧化鋁和氫氧化鈉反應(yīng)的化學(xué)方程式:NaOH+Al(OH)3=NaAlO2+H2O。氫氧化鋁是用量最大和應(yīng)用最廣的無(wú)機(jī)阻燃添加劑。氫氧化鋁作...

鎂在二氧化碳中燃燒的化學(xué)方程式:2Mg+CO2=點(diǎn)燃=2MgO+C。鎂是一種輕質(zhì)有延展性的銀白色金屬。是地球的地殼中第八豐富的元素,亦是宇宙...